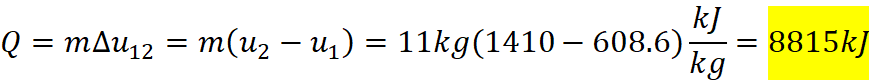TESTO DEL PROBLEMA:
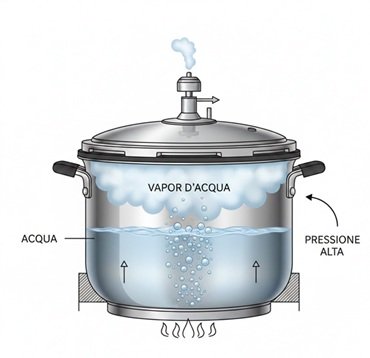
Una pentola a pressione contiene una miscela satura liquido-vapore. Si suppone contenga 10kg d’acqua e 1 kg di vapore inizialmente alla pressione di 1 atm e temperatura 100°C.
Calcolare la quantità di calore necessario fornire alla pentola per portare la miscela satura alla pressione di 5 bar.
SOLUZIONE DEL PROBLEMA:
Diagramma p-v mostra la trasformazione termodinamica subita dal sistema quando si somministra calore a volume specifico costante.
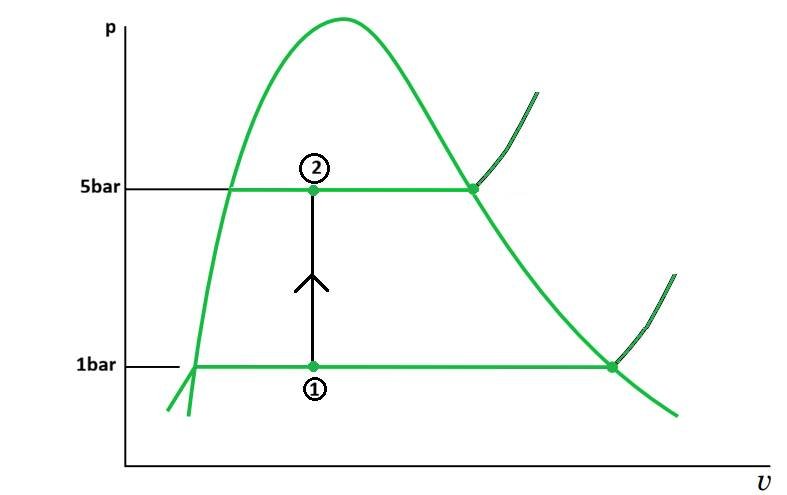
Poiché il nostro sistema è la pentola che è un sistema chiuso, applicando il Primo Principio della Termodinamica si ottiene la forma del calore ceduto alla miscela satura per arrivare a 5 bar a partire da 1bar:
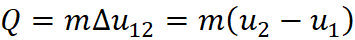
Le incognite del problema sono u2 e u1 e si ottengono esplicitando la formula del titolo di vapore per l’energia interna.
Il titolo di vapore del primo stato termodinamico è calcolabile dalla conoscenza delle masse d’acqua e vapore:
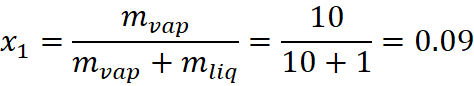
Sfruttando che la trasformazione è un’isocora quindi v1=v2 si può arrivare a calcolare il titolo di vapore dello stato termodinamico 2 e successivamente l’energia interna:
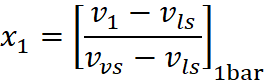
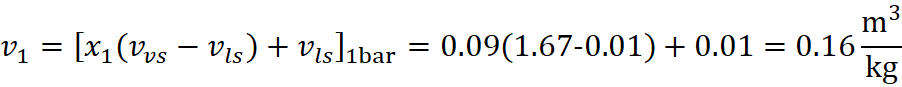
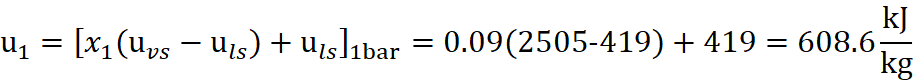
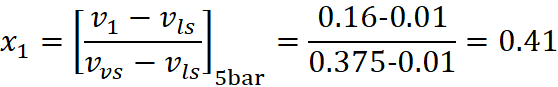
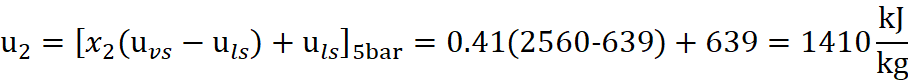
Da cui si ottiene il calore necessario: